1. Взаимодействие на аминокиселини с азотиста киселина.
За аминокиселините са характерни много общи реакции, в които участват техните карбоксилна или алфа-аминогрупа, като например взаимодействието им с азотиста киселина, с формалдехид, с метални йони, нинхидриновата реакция и др. Някои от тези реакции се използват за количествено определяне на аминокиселите. Присъствието на аминогрупа на алфа-място във въглеродната верига на аминокиселините може да се докаже чрез взаимодействието и с азотиста киселина. Азотистата киселина е нетрайна и затова трябва да се получи в момента на опита при взаимодействие на натриев нитрат със силна киселина, например азотна. Получената азотиста киселина окислява аминогрупата на аминокиселината, при което се отделя азот.
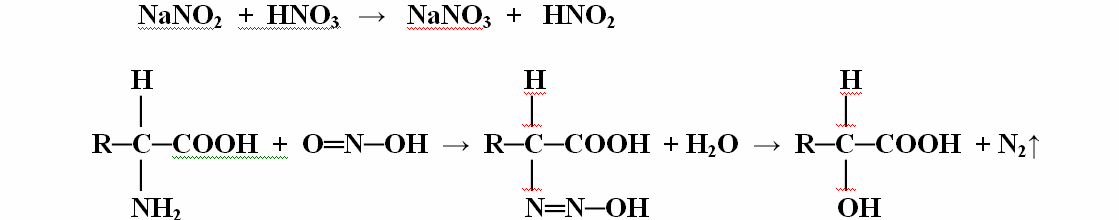
На тази реакция се основава метод за количествено определяне на аминокиселини в непознат разтвор, като се измерва обемът на отделящия се азот.
2. Нинхидринова реакция.
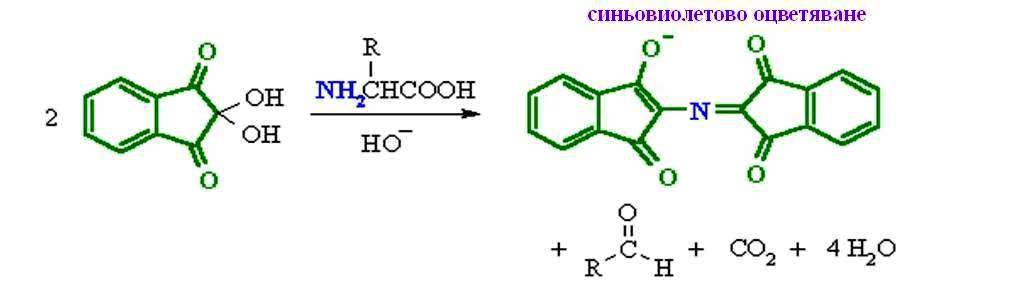
Характерна е само за алфа аминокиселините. При нагряване с нинхидрин
алфа аминокиселините се окисляват и се разпадат на алдехид, въглероден диоксид и амоняк, при което се образува съединение със синьовиолетов цвят. Реакцията с нинхидрин се използва за откриване и количествено определяне на аминокиселините.
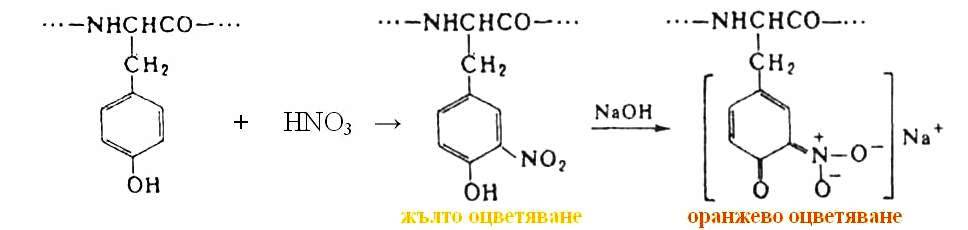
3. Ксантопротеинова реакция.
Характерна е за ароматните аминокиселини, които при загряване с концентрирана азотна киселина дават жълто оцветяване, което преминава в оранжево при прибавяне на основа или на амоняк. При взаимодействие с концентрирана азотна киселина бензолните ядра на ароматните аминокиселини се нитрират и се образуват нитросъединения с жълт цвят. При алкализиране нитросъединенията образуват оранжево оцветени хиноидни производни. Освен аминокиселините и белтъците ксантопротеинова реакция дават и много други ароматни съединения.
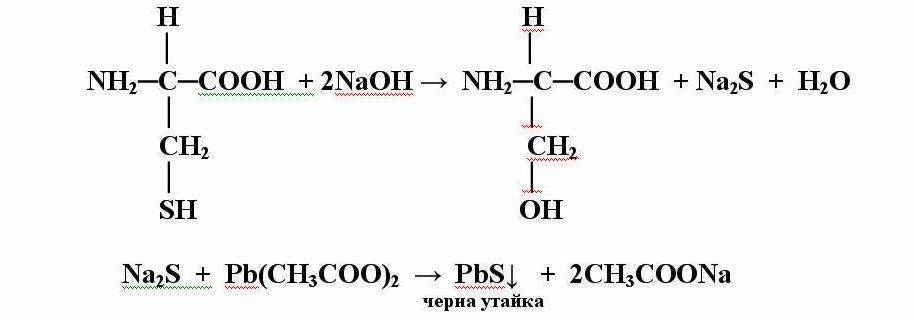
4. Реакция на Фол за сяросъдържащи аминокиселини.
При загряване на белтък (до кипене) с концентрирана натриева основа и
оловен ацетат разтворът започва да потъмнява. Концентрираната основа разрушава сяросъдържащите аминокиселини и отцепва сярата от белтъка.
 Указания за практическа работа:
Указания за практическа работа:
 1. Взаимодействие на аминокиселини с азотиста киселина
1. Взаимодействие на аминокиселини с азотиста киселина
А/ Необходими материали: к.HNO3, сух NaNO2 , разтвори на
алфа аминокиселини
Б/ Ход на анализа: В епруветки се наливат по 0,5 ml прясно
приготвен разтвор на натриев нитрит и по 0,6 ml концентрирана азотна киселина. В първата епруветка се прибавя 0,5 ml вода, а в другите същото количество от разтворите на аминокиселините.
2. Нинхидринова реакция
А/ Необходими материали: 0,2%-ов разтвор на нинхидрин в етанол, разтвори на алфа аминокиселини.
Б/ Ход на анализа:
Зарежда се контролната епруветка, в която вместо разтвор на аминокиселина се налива 1 ml вода. В останалите епруветки се наливат по 1 ml от разтворите на аминокиселини. Към всяка епруветка се прибавят се по 5—6 капки разтвор на нинхидрин и епруветките се загряват на спиртна лампа внимателно, като се разклащат леко. Появява се синьо оцветяване при наличие на алфа аминокиселини.
Методът може да се използва и за снемане на пръстови отпечатъци.Неговата изключителна химическа чувствителност към аминокиселините на потта го налага като едно от основните средства в криминалистическата практика.
Методът се използва за проявяване на следи върху порести повърхности – хартия, картон, необработено дърво и др. Проявените следи имат виолетов цвят. Работният ацетонов разтвор на нинхидрина е с концентрация 0,2 до 0,3 % в зависимост от давността на следата. За по-стари следи се използва по-висока концентрация на разтвора. Той се нанася върху изследваната повърхност чрез тампон, пулверизатор или потапяне в него на самата повърхност. За ускоряване процеса на проявяването от 20–30 минути до няколко часа се практикува загряване на обекта с ютия.
Нинхидриновият разтвор има предимства над другите химически разтвори-проявители, защото с него могат да се проявяват следи с много голяма давност. Известни са случаи на проявяване на следи, оставени върху архивни документи преди повече от десет години.
3. Ксантопротеинова реакция
А/ Необходими материали: 0,1%-ов воден разтвор на фенол (C6H5OH), к.HNO3, 20%-ов воден разтвор на NH3 или NaOH, разтвори на
алфа аминокиселини.
Б/ Ход на анализа: Зарежда се контролнат епруветка, в която вместо разтвор на аминокиселина се налива същото количество вода. В останалите епруветки се наливат по 1 ml от разтворите на аминокиселини. В последната епруветка се налива 1 ml разтвор на фенол. Към всички епруветки се прибавя 1 ml концентрирана азотна киселина. Внимателно се загрява! При наличие на съединения с бензолно ядро се появява жълто оцветяване. Епруветките от опитите се оставят да изстинат и внимателно в тях се прибавя по няколко капки разтвор на амоняк или на натриева основа. Под действие на основата жълтият цвят преминава в оранжев.
 4. Реакция на Фол за сяросъдържащи аминокиселини
4. Реакция на Фол за сяросъдържащи аминокиселини
А/ Необходими материали: 0,5%-ов разтвор на оловен ацетат (Pb(CH3COO)2 ), 10%-ов воден разтвор на NaOH, разтвори на алфа аминокиселини.
Б/ Ход на анализа: В епруветки се налива по 1 ml разтвор на оловен ацетат. На капки се налива разтвор на натриева основа, докато се разтвори образуващата се утайка. В контролната епруветка се прибавят няколко капки вода, а в останалите от разтворите на алфа аминокиселините. Епруветките внимателно се загряват! Разтворът в опитните епруветки, в които се съдържат сяросъдържащи аминокиселини започва да потъмнява.
Здравословни и безопасни условия на труд

 1. NaOH е силно корозивна. Предизвиква тежки изгаряния. Може да предизвика сериозни трайни увреждания на очите. Опасна е при поглъщане, контакт с кожата или при вдишване на прах.
1. NaOH е силно корозивна. Предизвиква тежки изгаряния. Може да предизвика сериозни трайни увреждания на очите. Опасна е при поглъщане, контакт с кожата или при вдишване на прах.

 2. Азотната киселина (HNO3) може да бъдат фатална при поглъщане или вдишване. Изключително е корозивна. При контакт с кожата или очите може да предизвика тежки изгаряния и трайно увреждане. Експериментът трябва да се изпълнява в камина!
2. Азотната киселина (HNO3) може да бъдат фатална при поглъщане или вдишване. Изключително е корозивна. При контакт с кожата или очите може да предизвика тежки изгаряния и трайно увреждане. Експериментът трябва да се изпълнява в камина!
При попадане върху кожата се образуват жълти петна, които са резултат от ксантопротеиновата реакция.
 3. Азотиста киселина(HNO2) – работи се в камина!
3. Азотиста киселина(HNO2) – работи се в камина!
Тя е нетрайна и се разлага на NO + NO2 + Н2О
NO – токсичен за централната нервна система и в по –големи дози превръща хемоглобина в метхемоглобин, ПДК 5 мг/l
NO2 – предизвиква отоци, понижава кръвното налягане, ПДК 9 мг/l
 4.Фенол - Водните му разтвори се използват за дезинфекция, поради силната си токсичност. Фенолът и производните му са протоплазмени отрови, които преципитират протеините в клеткитe. Освен това притежават висока повърхностна активност, защото в молекулата си съдържат липофилни и липофобни групи. При остро отравяне с фенол се прави стомашна промивка с 2% разтвор на натриев тиосулфат. Млякото, мазнините и алкохолът са противопоказани, тъй като улесняват резорбцията на фенола.
4.Фенол - Водните му разтвори се използват за дезинфекция, поради силната си токсичност. Фенолът и производните му са протоплазмени отрови, които преципитират протеините в клеткитe. Освен това притежават висока повърхностна активност, защото в молекулата си съдържат липофилни и липофобни групи. При остро отравяне с фенол се прави стомашна промивка с 2% разтвор на натриев тиосулфат. Млякото, мазнините и алкохолът са противопоказани, тъй като улесняват резорбцията на фенола.
 5. Спазвайте правилата за безопасна работа при нагряване със спиртна лампа.
5. Спазвайте правилата за безопасна работа при нагряване със спиртна лампа.
![]() Въпроси и задачи
Въпроси и задачи
1. Отчетете резултатите в табличен вид и направете изводи за съдържанието на аминокиселини в съответните проби.
2. Възможно ли е белтъчен разтвор да дава положителна нинхидринова реакция? Обосновете отговора си.
3. Какъв извод може да се направи за неизвестен разтвор, който дава отрицателна нинхидринова реакция и положителна ксантопротеинова?
4. Положителна ли е реакцията на Фол за всички разтвори даващи положителна нинхидринова проба? Обяснете резултатите.
 За любознателните:
За любознателните:
Повече за незаменимите аминокиселини можете да прочетете тук.
Повече за аминокиселините на английски език можете да прочетете тук.
Повече за аминокиселините на руски език можете да прочетете тук.



